Des cristaux contre le cancer
C’est un remarquable exemple de transfert direct d’une technologie de physique des particules vers la médecine. Un nouveau système de tomographie par émission de positons (TEP), dédié à l’imagerie du sein, démarre des essais cliniques au Portugal. Permettant de détecter des tumeurs plus petites et d’éviter des biopsies inutiles, il a été développé par un consortium portugais en collaboration avec le CERN et des laboratoires associés à la collaboration Crystal Clear.
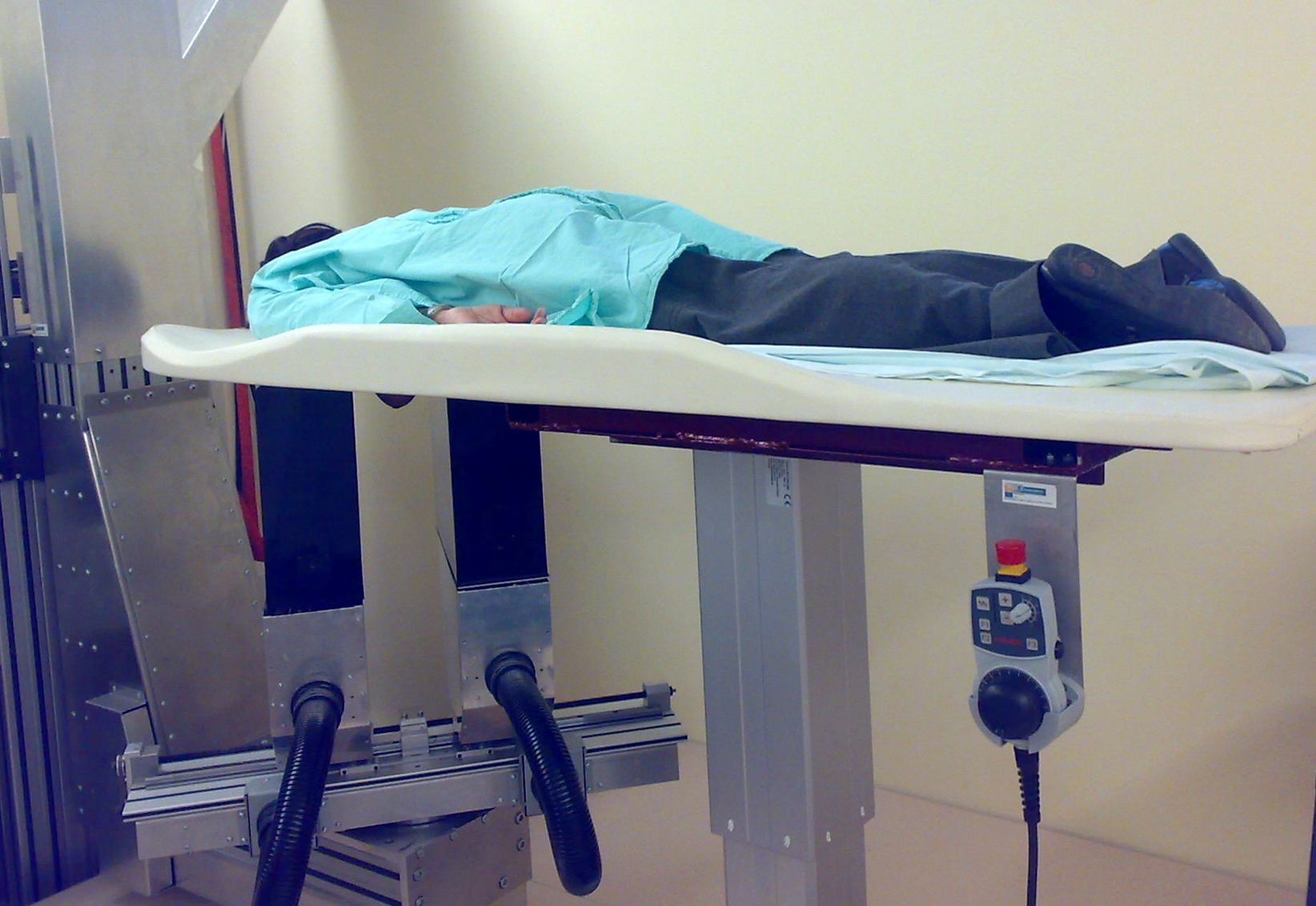

L’antimatière, ça sert… et pas seulement à faire des films ou des livres à succès. Un nouveau type d’appareil de tomographie par émission de positons (TEP) vient d’être mis en service, le premier du genre en Europe. Si les essais sont concluants, il promet de faire progresser le diagnostic du cancer du sein. En février, le consortium PET-Mammography, regroupant huit instituts portugais dont le Laboratoire de physique des particules du Portugal (LIP), l’Hôpital Garcia de Orta de Lisbonne et l’Institut d’oncologie de Porto, a mis en service un prototype de TEP dédié à l’imagerie du sein pour des essais cliniques. Cet appareil a été développé au cours des cinq dernières années dans le cadre de la collaboration Crystal Clear. La collaboration Crystal Clear, dont le porte-parole est Stefaan Tavernier de l’Université Vrije Universiteit de Bruxelles, mène depuis 1990 des travaux sur les cristaux pour la physique des particules et leurs applications au-delà.
Jusqu’à présent, les appareils de tomographie par émission de positons (TEP) se présentent comme de grosses machines capables de «photographier» l’ensemble du corps (voir ci-dessous). Mais pour obtenir de meilleures performances, les membres de la collaboration Crystal Clear ont eu l’idée il y a quelques années de développer des appareils TEP dédiés. L’imagerie du sein est vite apparue comme bien appropriée: le sein est un organe «externe», qui peut plus facilement être «placé» dans un tel appareil. De plus, il y a de réels besoins en la matière: si leur résolution spatiale est excellente, les mammographies classiques par rayons X donnent souvent des résultats indécis. «60 % des images donnant un résultat positif, qui indiquent donc un problème possible, ne sont en réalité pas des cancers», indique Paul Lecoq, physicien de CMS et initiateur de la collaboration Crystal Clear. En particulier, les mammographies réalisées sur des femmes jeunes, qui présentent des tissus mammaires denses, sur des femmes qui ont subi de la chirurgie plastique ou sur celles qui suivent un traitement contre la ménopause, peuvent donner des résultats faussés. Le médecin prescrit alors une biopsie: même s’il est léger, cet acte chirurgical n’est pas anodin, et il est de surcroît coûteux.
Pour ces patientes, le nouvel appareil ClearPEM (PEM pour mammographie par émission de positons) peut réaliser des prouesses et éviter des biopsies inutiles. «Des millions de patientes en Europe sont concernées», indique Paul Lecoq. L’intérêt par rapport à un appareil TEP classique est également patent. Le ClearPEM est plus sensible que le TEP, détectant 5 à 10 fois plus de rayonnements émis par rapport à une même dose injectée (voir ci-dessous). Cette meilleure sensibilité se traduit par la détection de tumeurs plus petites: il peut identifier des tumeurs de 2 à 3 millimètres de diamètre, contre 10 à 15 millimètres pour un TEP «corps entier». L’examen est plus rapide. «Il peut être réalisé en 5 minutes au lieu de 25 avec un TEP classique», explique Joao Varela, physicien de CMS qui dirige par ailleurs la collaboration portugaise sur le ClearPEM. Examen plus rapide signifie moins de dose radioactive injectée.
Le défi était donc de rendre un appareil TEP assez compact pour être dédié à un organe. Les développements ont débuté en 2003, avec l’aide des techniques utilisées pour le calorimètre électromagnétique de CMS. «Le ClearPEM est exactement comme un calorimètre électromagnétique à cristaux. La seule différence, c’est la taille! », souligne Joao Varela. Le ClearPEM est à ce titre un formidable exemple de transfert direct de la physique des particules vers la médecine.
L’appareillage consiste en deux plaques de 16 par 18 cm, dotées de cristaux et insérées avec l’électronique dans un châssis robotisé. Pendant l’examen, l’appareillage tourne autour du sein. Comme le calorimètre de CMS, le ClearPEM est doté de cristaux qui scintillent au passage des photons de haute énergie (rayons gamma) émis par le corps. Les 6000 cristaux du ClearPEM sont cependant bien plus sensibles que ceux de CMS car ils doivent détecter des signaux bien plus faibles. Et ils sont bien entendu bien plus petits car les énergies des rayons gamma à détecter sont environ 100000 fois plus faibles. Ils ont été caractérisés au CERN par un appareil similaire à celui utilisé pour les cristaux de CMS.
L’une des clés pour rendre l’appareil compact a été l’utilisation des photodiodes à avalanches (APD) qui transforment le signal lumineux en signal électrique. Ces carrés de silicium très compacts, qui se collent à l’extrémité du cristal, ont été développés pour CMS. «Nous avons également dû mettre au point une électronique à très bas bruit et très compacte, ainsi qu’une électronique de lecture qui s’est inspirée du système de déclenchement de CMS», poursuit Joao Varela. Il faut dire que Joao Varela n’est autre que… le responsable du système de déclenchement de CMS!
Le prototype est désormais utilisé pour réaliser 100 à 200 des essais cliniques à l’Institut d’oncologie de Porto. En fonction des résultats obtenus, la communauté médicale pourra décider d’utiliser un tel appareil. Mais en attendant, les membres de la collaboration Crystal Clear ont d’autres projets dans les cartons, notamment dans le cadre du projet CERIMED. Le projet CERIMED (Centre européen de recherche en imagerie médicale), qui s’installe à Marseille sous l’impulsion de son promoteur, Paul Lecoq, construit un appareil TEP couplé à un système à ultrasons. Baptisé ClearPEM sonic, ce nouvel appareil sera installé d’ici à la fin de l’année à l’Hôpital de la Timone à Marseille. Les technologies TEP et ultrasons couplées promettent encore d’améliorer l’imagerie du sein.
Comment fonctionne un appareil TEP?
La tomographie par émission de positons (TEP) est une méthode d’imagerie médicale qui permet de mesurer en trois dimensions l’activité métabolique d’un organe. On injecte au patient un sucre marqué par un produit radioactif. Les cellules cancéreuses, qui ont une plus grande activité que les cellules saines, vont en priorité absorber ce sucre un peu particulier, qui n’est pas métabolisé par les cellules. Le marqueur radioactif, du Fluor 18, se désintègre en émettant des positons (les antiparticules des électrons) qui s’annihilent à leur tour en émettant en directions opposées deux rayons gamma (photons) d’une énergie déterminée (511 keV). Les cristaux de l’appareil TEP, disposés sur deux plaques placées de chaque côté du corps ou de l’organe, détectent ces paires de photons, comme le calorimètre à cristaux de CMS détectera les deux rayons gamma issus de la désintégration du boson de Higgs! En reconstituant toutes les coïncidences (les deux photons émis en même temps en sens opposés), l’appareil reconstruit une image qui permet d’observer le métabolisme des cellules. C’est pourquoi on parle d’imagerie fonctionnelle par opposition aux techniques d’imagerie par rayons X, par exemple, qui donnent une vision anatomique.

